 CULTURA|CIENCIA
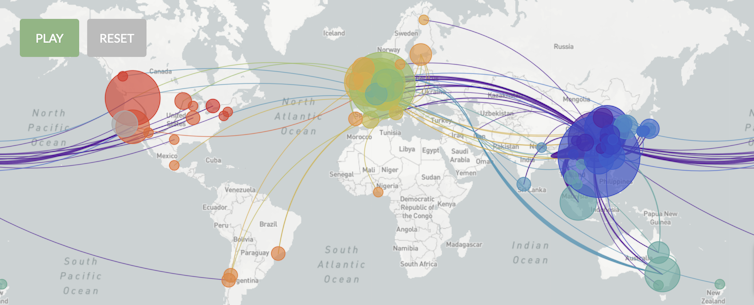
Epidemiología genómica del nuevo coronavirus (hCoV-19) construida con nextstrain/ncov utilizando datos de Gisaid. nextstrain.org
CULTURA|CIENCIA
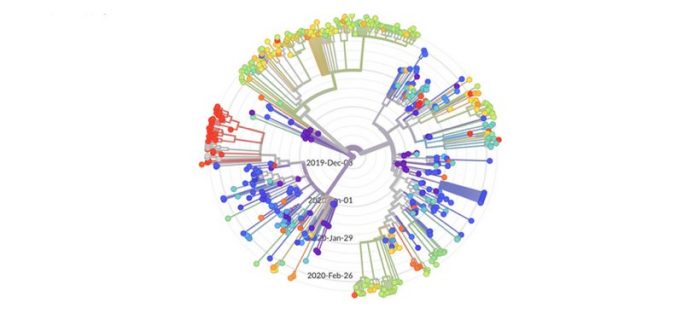
Epidemiología genómica del nuevo coronavirus (hCoV-19) construida con nextstrain/ncov utilizando datos de Gisaid. nextstrain.org
¿De qué sirve secuenciar el coronavirus?
Algunos virus, entre ellos patógenos muy importantes como el de la gripe, la hepatitis C o el VIH, tienen un genoma de ARN. Es decir, con una base diferente: U en vez de T. Pero el código con el que se interpretan las instrucciones es el mismo, cambiando solo la T por la U. Esto posibilita que un virus de ARN pueda “secuestrar” la maquinaria molecular de una célula humana y obligarle a copiar y ejecutar sus instrucciones en vez de las de la propia célula.
Hace unos días, científicos de la Universitat de València y de FISABIO hemos obtenido y publicado las primeras secuencias del genoma completo del coronavirus SARS-CoV-2 de pacientes españoles. Nos hemos unido a un numeroso grupo de investigadores de todo el mundo que, desde prácticamente el inicio de la pandemia de COVID-19, comparten la información genética de este virus.
Entre las numerosas preguntas que nos planteamos estos días sobre esta enfermedad y el virus que la causa, vamos a intentar responder a una más: ¿para qué sirve secuenciar el genoma del coronavirus?
De la biología básica a la evolución
El genoma de cualquier organismo, virus incluidos, son las instrucciones moleculares, en forma de nucleótidos, necesarias para su funcionamiento y la transmisión a la descendencia. La mayoría de organismos (incluidas las bacterias y muchos virus) tienen un genoma con un código formado por 4 nucleótidos. Las conocidas bases del ADN: A, C, G y T.
Algunos virus, entre ellos patógenos muy importantes como el de la gripe, la hepatitis C o el VIH, tienen un genoma de ARN. Es decir, con una base diferente: U en vez de T. Pero el código con el que se interpretan las instrucciones es el mismo, cambiando solo la T por la U. Esto posibilita que un virus de ARN pueda “secuestrar” la maquinaria molecular de una célula humana y obligarle a copiar y ejecutar sus instrucciones en vez de las de la propia célula.
No solo eso. Además de portar las instrucciones para funcionar y transmitirse, el genoma actúa como archivo histórico de la evolución. Esto quiere decir que los cambios, las mutaciones que permiten que los organismos cambien y se adapten a su ambiente, son en realidad cambios en las bases nucleotídicas. Por ejemplo, si donde antes había una A aparece ahora una T, es posible que se altere una proteína, que el organismo pierda (o gane una función) o se altere la regulación del desarrollo de un embrión. Aplicando modelos matemáticos y bioinformáticos, podemos reconstruir la historia evolutiva de cualquier grupo de organismos actuales comparando sus secuencias genómicas.
La secuencia del genoma tiene múltiples aplicaciones
Aunque en los últimos años hemos oído hablar bastante de la secuenciación de genomas para la medicina personalizada, para la búsqueda de genes asociados a enfermedades neurodegenerativas o para detener la progresión de tumores, casi siempre nos referimos al genoma humano. Pero la realidad es que también secuenciamos, y en gran cantidad, los genomas de microorganismos patógenos.
En este caso, los genomas nos aportan otro tipo de información. Seguiré un orden cronológico sobre el desarrollo de la epidemia para ver qué nos aporta primero una y luego muchas secuencias del genoma del coronavirus.
El primer genoma de SARS-CoV-2 se obtuvo en Wuhan, a finales de diciembre de 2019. Esto permitió identificar al virus como un coronavirus y comprobar que era diferente a los otros coronavirus conocidos. El análisis evolutivo demostró que estaba emparentado con virus cuyo hospedador primario son especies de murciélagos, lo que llevó a postular que éstos son también el reservorio original del SARS-CoV-2.
Sin embargo, tanto el SARS-CoV como el MERS-CoV (los otros dos coronavirus que han causado brotes epidémicos recientemente) saltaron a la especie humana a través de especies intermediarias, civetas y camellos, respectivamente, lo que hace sospechar que lo mismo ha sucedido en el origen del COVID-19. Aún no se ha identificado ese hospedador intermediario.
El análisis comparado del genoma con el de otros virus permite identificar qué mutaciones hacen diferente al SARS-CoV-2 y cuáles le asemejan a otros virus. Esto nos permite buscar dianas terapéuticas, entender cómo entra el virus en las células o explicar por qué afecta más a hombres que a mujeres.
Ya está mutando
Gracias a la elevada tasa de mutación de los virus con genoma de RNA, los cambios en sus genomas se acumulan en cuestión de días. Aunque el ritmo de evolución del SARS-CoV-2 es más lento que el de la gripe o el VIH, aún es lo bastante rápido para que podamos observar las mutaciones acumuladas desde que se produjeron las primeras infecciones en Wuhan. Para hacerlo es preciso comparar las secuencias de muchos virus y, para ello, es esencial poder acceder a la información que se va generando desde distintos rinconces del mundo.
Esto se realiza gracias a la colaboración desinteresada de muchos científicos, que comparten las secuencias que obtienen en una plataforma establecida previamente para la vigilancia de la gripe (GISAID, siglas de Global Initiative on Sharing All Influenza Data. Los datos genómicos en bruto son imprescindibles, pero aún más su análisis en tiempo real, que es posible gracias a un programa que aprovecha los datos de GISAID para establecer las rutas de transmisión del virus.
Al igual que estudiamos la evolución a largo plazo, a corto plazo podemos estudiar la epidemiología según los virus. Tenemos así, una potentísima herramienta, para contrastar los resultados de la epidemiología clásica, basada en el estudio de contactos, y fortalecer las medidas de control de la epidemia y su efectividad.